학문
고분자물질의 극성 비극성 구분하는 방법
고분자는 극성을 어떻게 구별할 수 있나요? 화학식보고 구조 예측해서 알아볼 수 있는건가요? 아니면 친수성 소수성만 보고 극성 비극성으로 구분하나요??
3개의 답변이 있어요!
안녕하세요.
고분자 물질의 극성과 비극성을 구분하는 가장 쉬운 방법은 그 물질을 이루는 원소의 종류와 분자의 결합 구조를 살펴보는 것이에요. 일반적으로 산소, 질소, 염소처럼 전자를 강하게 끌어당기는 원자가 포함되어 있다면 분자 내에 전하의 불균형이 생겨 극성을 띠게 됩니다. 우리가 흔히 사용하는 페트병이나 의류용 나일론 등이 대표적인 극성 고분자인데, 이런 물질들은 다른 극성 용매나 접착제와 비교적 잘 반응하는 특징을 가지고 있어요.
반대로 탄소와 수소로만 사슬이 구성된 폴리에틸렌이나 폴리프로필렌은 전자가 어느 한쪽으로 치우치지 않아 비극성 성질을 나타내게 되지요. 이때 분자의 대칭성도 매우 중요한데, 아무리 극성 원자가 있더라도 구조가 완벽하게 대칭을 이루면 전체적인 극성은 서로 상쇄되어 사라지게 된답니다. 실생활에서 이를 확인하려면 표면 장력을 이용해 물방울을 떨어뜨려 보세요. 물방울이 흡수되지 않고 동그랗게 맺히면 비극성, 표면에 넓게 퍼지면 극성 물질일 확률이 매우 높으니 이를 참고하시면 큰 도움이 될 거예요.
감사합니다.
안녕하세요. 김찬우 전문가입니다.
고분자의 극성 비극성을 파악하는 것은 구조도 보고 친수성기 소수성기가 있는지 둘다 봐야 합니다.
먼저 화학식에서 전기음성도가 큰 F, Cl 과 같은 작용기가 있으면 극성일 확률이 높습니다.
그리고 작용기에 C, H 만으로 이루어진 고분자의 경우는 대칭이라 비극성일 확률이 높습니다.
그리고 실제로 물질이 있다면 물이나 알콜에 잘 녹거나 반응하면 극성이고 반응을 하지 않으면 비극성으로 판정을 할 수도 있습니다.
그럼 답변 읽어주셔서 감사드립니다~! 더 궁금한게 있으시면 언제든지 문의 주십시요:)
안녕하세요, 미소짓는자스민님. 이중철 과학기술전문가입니다.
먼저, 고분자 물질이 '극성(Polar)'인지 '비극성(Non-polar)'인지 구분하는 것은 질문자님이 이미 배웠거나 앞으로 배우게 될 화학의 기본 원리인 '전하의 치우침' 개념을 이해하면 아주 쉽습니다. 화학식 구조를 보는 법과 성질로 구분하는 법을 이해하기 쉽게 정리해 드리겠습니다.1. [가장 정확한 방법] 화학식과 구조로 예측하기!!
고분자는 수천, 수만 개의 원자가 연결되어 있지만, 결국 '단량체(모노머, 작은 기본 단위)'가 반복되는 구조입니다.
따라서, 단량체의 구조를 보면 극성 여부를 알 수 있게 되는 것이지요.
1) 전하의 '줄다리기'를 보세요. (핵심: 쌍극자 모멘트)
원자들 사이에는 전자를 끌어당기는 힘(전기음성도)의 차이가 있습니다.
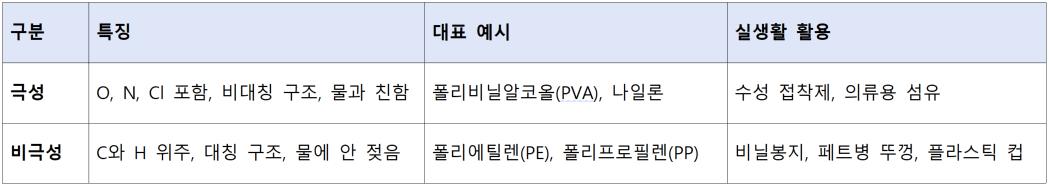
극성: 구조 내에 산소(O), 질소(N), 염소(Cl)처럼 전자를 강하게 끌어당기는 원자가 한쪽으로 치우쳐 있을 때입니다.
비극성: 구조가 매우 대칭적이라서 전자를 당기는 힘이 사방에서 상쇄될 때입니다. (Ex. 폴리에틸렌)
2) 특정 '편을 가르는 팀원'이 있는지 확인하세요. (핵심: 작용기)
화학식에 다음과 같은 모양이 보인다면 대부분 극성입니다.
참고로, 자주 보이는 것은 이해를 바탕으로 외워두면 편하겠지요?
-OH(히드록시기): 산소가 전자를 확 끌어가서 강한 극성을 띱니다. (Ex. PVA)
-COOH(카르복실기): 식초처럼 시큼한 성질을 내며 극성이 강합니다.
-Cl(염소): 한쪽에서 전자를 세게 당깁니다. (Ex. PVC)
반면에, 탄소(C)와 수소(H)로만 이루어져 있다면 거의 100% 비극성입니다. (Ex. 비닐봉지인 PE, 플라스틱 용기인 PP)
2. '친수성·소수성'과 '극성·비극성'의 관계
질문하신 것처럼 이 둘은 아주 밀접한 관계가 있습니다.
하지만, 각 정의는 조금 다르다는 것을 구분하여 숙지해야 한답니다.
극성/비극성: 분자 내부에 전기가 치우쳐 있는가 하는 '상태'입니다.
친수성/소수성: 물(H₂O)과 친한가 하는 '성향'입니다.
※ 핵심 원리: 끼리끼리 녹는다?!
물은 대표적인 극성 물질입니다.
그래서 극성 고분자는 물과 친하고(친수성), 전기가 치우치지 않은 비극성 고분자는 물을 싫어합니다(소수성).
따라서, 물에 잘 젖거나 녹는 고분자를 보며 '아, 이건 극성이겠구나!'라고 추측하는 것이야말로 아주 훌륭한 접근법입니다.
3. [대표적인 예시] 한눈에 비교하는 고분자!
정리하자면,
1) '화학식'을 볼 때:
산소(O)나 질소(N) 같은 원자가 한쪽에 툭 튀어나와 있거나 대칭이 깨져 있다면 극성입니다.
탄소와 수소만 가득하면 비극성입니다.
2) '성질'을 볼 때:
물을 뿌렸을 때 물방울이 퍼지지 않고 동글동글 맺히면(소수성) 비극성, 물이 쫙 퍼지며 스며들면(친수성) 극성일 확률이 매우 높다고 판단할 수 있습니다.
즉, 화학 구조를 먼저 보고, 그 구조 때문에 나타나는 성질(친수성·소수성)을 연결해서 이해할 수 있다면, '화학'이 훨씬 쉽고 흥미있게 느껴질 거에요.