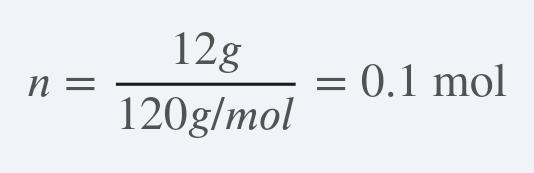학문
더없이공부하는깍두기
화학 2 (몰농도, 몰랄농도)문제 질문입니다.
화학 2 문제 질문입니다.
정답이 1번이라 하는데 어떻게 풀어야 1번이 나오는건가요?식 풀이도 함께 포함해서 해설해주세요..
2개의 답변이 있어요!
안녕하세요. 이중철 전문가입니다.
질문하신 화학2 문제는 용액의 세 가지 농도 단위(퍼센트 농도, 몰랄 농도, 몰농도)를 비교하고 이를 통해서 이해하는 아주 좋은 문제 유형이니, 천천히 풀이 내용을 익혀보면서 이해에 도움이 되기를 바랄게요.
1. 먼저, 문제에서 공통적으로 주어진 정보부터 함께 정리해 볼까요?
용질 A의 질량: 12g
용질 A의 분자량: 120
용질 A의 몰수(n):
(즉, 모든 비커에는 용질 A가 똑같이 0.1몰씩 들어있습니다.)
2. 이제부터, 각 용액의 상태 파악해 볼게요.
(가) 10% 수용액
정의: (용질 질량 / 용액 질량) × 100
계산: 10% = (12g / 용액 질량}) × 100
용액의 총 질량: 120g
물(용매)의 질량: 120g - 12g = 108g
(나) 1m (몰랄 농도) 수용액
정의: 용매(물) 1kg(1000g)에 녹아있는 용질의 몰수
계산: 1m = 0.1mol / 물 질량(kg)
물(용매)의 질량: 0.1kg = 100g
용액의 총 질량: 100g + 12g = 112g
(다) 1M (몰농도) 수용액
정의: 용액 1L(1000mL)에 녹아있는 용질의 몰수
계산: 1M = 0.1\mol / 용액 부피(L)
용액의 부피: 0.1L = 100mL
용액의 총 질량: 밀도가 1.05g/mL이므로, 100mL × 1.05g/mL = 105g
물(용매)의 질량: 105g - 12g = 93g
3. <보기> 논리적 검토와 풀이는 아래와 같으니 집중!
ㄱ. 용액의 질량 비교
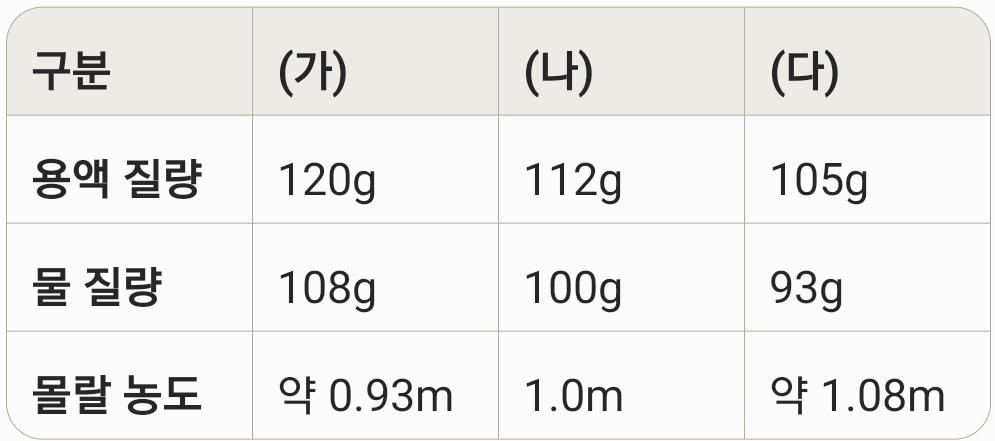
위에서 계산한 용액의 총 질량을 비교해 봅시다.
(가): 120g
(나): 112g
(다): 105g
결과: (다) < (나) < (가) 순서가 맞습니다. (ㄱ은 옳은 설명)
ㄴ. 용액의 몰랄 농도(m) 비교
몰랄 농도는 '똑같은 양의 용질(0.1mol)이 들어있을 때, 물(용매)의 양이 적을수록' 농도가 진해집니다.
물(용매)의 양 비교: (가) 108g > (나) 100g > (다) 93g
물 성분이 가장 적은 (다)가 가장 진한 몰랄 농도를 가집니다.
정확한 농도 순서: (가) < (나) < (다)
보기에서는 (다) < (나) < (가)라고 했으므로 틀렸습니다. (ㄴ은 틀린 설명)
ㄷ. 용액의 끓는점 비교
용액의 끓는점 오름(델타 T_b)은 몰랄 농도(m)에 비례합니다. 즉, 몰랄 농도가 높을수록 끓는점도 더 높습니다.
위의 ㄴ에서 확인했듯이 몰랄 농도 순서는 (가) < (나) < (다)입니다.
따라서 끓는점이 가장 높은 것은 (다)입니다.
끓는점 순서: (가) < (나) < (다)
보기에서는 (다) < (나) < (가)라고 했으므로 틀렸습니다. (ㄷ은 틀린 설명)
4. 최종 결론을 내볼까요?
따라서, 옳은 설명은 ㄱ 하나뿐인 것이랍니다.
정답: ① ㄱ
《이해를 돕는 한 줄 요약》
"용질의 양이 12g으로 모두 같을 때, 전체 용액의 무게는 (가)가 가장 무겁고, 반대로 농도(몰랄 농도)는 물이 가장 적게 들어간 (다)가 가장 진하다"라고 이해하시면 완벽합니다!
채택 보상으로 291베리 받았어요.
채택된 답변안녕하세요.
몰농도는 용액 1L당 용질의 양을, 몰랄농도는 용매 1kg당 용질의 양을 나타내는 단위예요.
몰농도는 온도가 변하면 용액의 부피가 달라져 농도값도 변하지만, 몰랄농도는 질량 기준이라 온도와 무관하게 일정하다는 특징이 있죠.
두 농도를 서로 환산할 때는 용액의 밀도를 활용해 부피와 질량 사이의 관계를 파악하는 것이 가장 핵심적인 풀이 요령이랍니다.
공부하다 헷갈리는 부분이 있으면 언제든 다시 질문해 주세요.
감사합니다.